A Pfizer/BioNTech enviou neste sábado (6/2) à Agência Nacional de Vigilância Sanitária (Anvisa) o pedido para o registro definitivo da vacina COMIRNATY, contra a covid-19. A empresa é a segunda farmacêutica a avançar dessa forma no Brasil. A primeira foi a Fundação Oswaldo Cruz (Fiocruz) com a vacina de Oxford.
Quando finalizado, o registro concedido pela Anvisa será o sinal verde para que a vacina seja comercializada, distribuída e utilizada pela população, nos termos da indicação estabelecida na bula.
A farmacêutica anunciou que sua vacina contra a covid-19 é segura e tem 95% de eficácia. A vacina foi testada em 43,5 mil pessoas de seis países e, em setembro, a Anvisa (Agência Nacional de Vigilância Sanitária) autorizou que seus testes clínicos fossem ampliados no Brasil, de mil para dois mil testes em voluntários. Os testes foram feitos em São Paulo e Bahia.
O Brasil adquiriu, até o momento, 46 milhões de doses da vacina do Instituto Butantan em parceria com a farmacêutica Sinovac, com opção de compra de mais 54 milhões. O país recebeu também, da Índia, 2 milhões de doses da Astrazeneca, com opção de importação de mais doses, além de previsão de produção, pela Fundação Oswaldo Cruz (Fiocruz), de 100,4 milhões de doses no primeiro semestre e 110 milhões de doses no segundo semestre.
Há ainda, segundo o ministério, a possibilidade de aquisição de 42,5 milhões de doses pelo mecanismo Covax Facility, articulado pela Organização Mundial da Saúde (OMS).

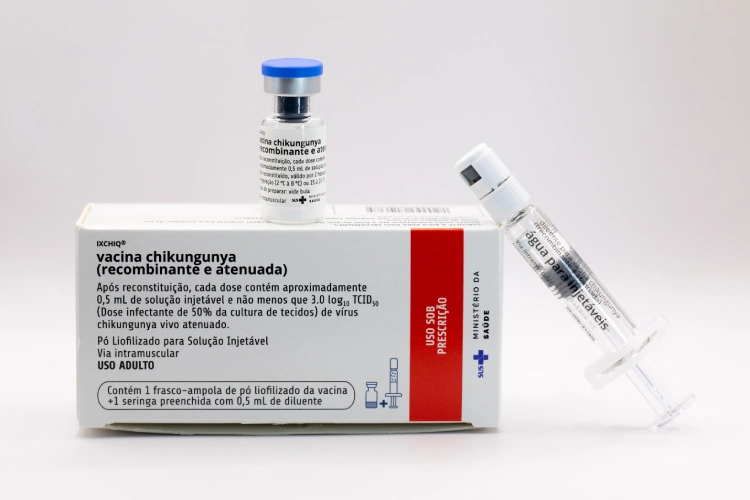 IMUNIZAÇÃO Vacinação contra chikungunya é adiada e deve começar só em junho em Sete Lagoas
IMUNIZAÇÃO Vacinação contra chikungunya é adiada e deve começar só em junho em Sete Lagoas  SETE LAGOAS Saúde abre processo seletivo para médicos especialistas em Sete Lagoas
SETE LAGOAS Saúde abre processo seletivo para médicos especialistas em Sete Lagoas 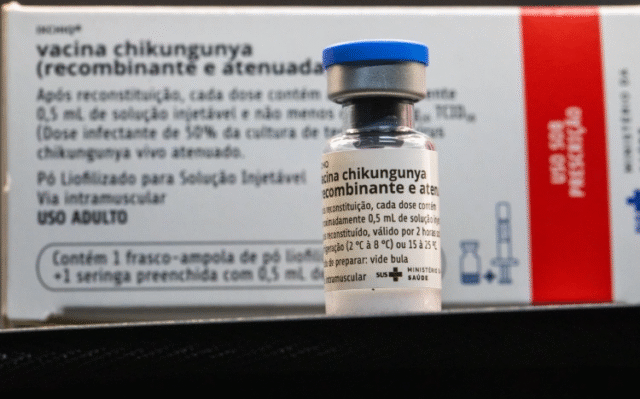 IMUNIZAÇÃO Sete Lagoas aguarda vacinas para iniciar campanha contra chikungunya
IMUNIZAÇÃO Sete Lagoas aguarda vacinas para iniciar campanha contra chikungunya Mín. 18° Máx. 25°