A vacina contra a Covid-19 totalmente brasileira, com insumos desenvolvidos no país – inclusive, o ingrediente farmacêutico ativo (IFA)–, deve começar a ser testada em humanos no segundo semestre deste ano. A informação é da professora Ana Paula Fernandes, coordenadora do Centro de Tecnologia em Vacinas (CT-Vacinas) da UFMG e da Rede Vírus, do Ministério da Ciência, Tecnologia, Inovações e Comunicações (MCTIC).
“Já estamos em intenso trabalho com a equipe da Fundação Ezequiel Dias (Funed), em interação com a equipe da Agência Nacional de Vigilância Sanitária (Anvisa), para que tudo seja feito de acordo com as exigências. Vamos fazer tudo para acelerar ao máximo e iniciar os testes clínicos no segundo semestre”, sinalizou a cientista.
Tecnologia
A avaliação de possíveis alternativas de vacinas contra o novo coronavírus, diz a pesquisadora, teve início na UFMG em fevereiro de 2020, quando a pandemia chegava ao país. Ana Paula Fernandes revela que foram testadas várias plataformas – nos ensaios das fases 1 e 2 da pesquisa, em camundongos – e obtidos “resultados excelentes com proteínas recombinantes”.
Essa plataforma, explica, é a mesma usada, por exemplo, em vacinas contra o HPV e a hepatite. Consiste na produção de proteínas recombinantes sintetizadas em organismos que não são os agentes causadores dessas doenças.
“Toda a base, inclusive os insumos mais importantes, foi desenvolvida aqui. Nas vacinas, em geral, o IFA precisa de vários componentes; um é o antígeno. Há vacinas que precisam de adjuvantes, para potencializar a resposta imune. Estamos fazendo um esforço para produzir tudo aqui”
Ana Paula Fernandes - Pesquisadora
A tecnologia é semelhante à adotada no imunizante da Universidade de Oxford, em parceria com a empresa AstraZeneca, que opera com vetores virais (vírus não patogênicos para os seres humanos) capazes de codificar proteínas do novo coronavírus sem causar a doença, mas estimulando a produção de anticorpos e células de defesa.
Lote inicial
“Estamos desenvolvendo em parceria com a Funed o lote que vai ser usado para os testes clínicos”, informa ainda, lembrando que a UFMG elabora, mas não produz vacinas. “Vamos fazer todos os testes de segurança, de toxigenicidade, tudo o que é requerido pela Anvisa para aprovação”, frisa.
E mais:
A previsão da cientista Ana Paula Fernandes, do CT-Vacinas da UFMG, é a de que a fase de testes clínicos, que tem três etapas, leve entre seis e 10 meses. Nas etapas um e dois, explica ela, é testado um número menor de pessoas, avaliando se o imunizante induziu uma reação do sistema imune, como produção de anticorpos e ativação de células envolvidas na resposta celular.
Além disso, aponta, será verificado se a vacina não causa efeitos adversos graves – o nível de segurança do imunizante. Depois de atestado que desenvolve resposta imune e não causa efeitos graves, a pesquisa é ampliada para 10 mil, 20 mil pessoas.
O nome da vacina brasileira está em fase de decisão pelo CT-Vacinas, pela Funed e pelo Ministério da Ciência, Tecnologia, Inovações e Comunicações (MCTIC). Os recursos para as duas etapas iniciais de testes em humanos, cerca de R$ 20 milhões, viriam de financiamento federal. A despesa com o estágio final, ainda não calculada, precisará de captação, segundo a pesquisadora.

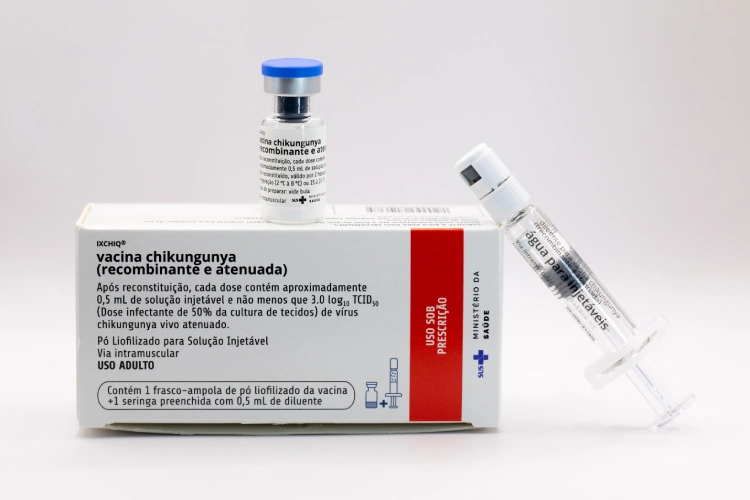 IMUNIZAÇÃO Vacinação contra chikungunya é adiada e deve começar só em junho em Sete Lagoas
IMUNIZAÇÃO Vacinação contra chikungunya é adiada e deve começar só em junho em Sete Lagoas  SETE LAGOAS Saúde abre processo seletivo para médicos especialistas em Sete Lagoas
SETE LAGOAS Saúde abre processo seletivo para médicos especialistas em Sete Lagoas  IMUNIZAÇÃO Sete Lagoas aguarda vacinas para iniciar campanha contra chikungunya
IMUNIZAÇÃO Sete Lagoas aguarda vacinas para iniciar campanha contra chikungunya Mín. 18° Máx. 25°